摘 要: 針對M型左心室的剖面超聲圖像進行研究。采用基于區域灰度擴展的CV水平集方法,通過限制能量擴展的方向,去除了相關的干擾,有效地提取了左心室的內外膜。在準確地提取了心肌邊界后,對左心室的相關特征進行了紋理變化分析。結果表明,心肌運動的過程中收縮期和舒張期的共生矩陣各特性參數、分形維等均有定量的差別,可將相關的紋理參數用于正常心肌與病變心肌的定量分析上,方便醫生進行準確的病理判斷。
關鍵詞: 超聲圖像;左心室;CV水平集;收縮和擴張
心功能的定量測定是臨床對超聲心動圖檢查的一個基本要求。但是由于超聲心動圖的圖像質量較差, 噪聲高、分辨率低、對比度低、邊界缺失和邊界不連續等阻礙了心功能超聲定量測定的發展。要對左心室心功能進行定量分析,準確地勾畫左心室的心內膜邊界則是首要條件[1],而較差的超聲圖像質量使心內膜面的勾畫變得很困難。KRIPS R[2]等提出了一種離散小波變換結合time-space算法來實現心肌組織與血液的鑒別,這樣不需要事先確定ROI區域,雖實現了鑒別但并沒有確切地提取出內膜的邊界;LACERDA S G[3]等提出了一個結合圖像處理技術的徑向搜索算法對左心室進行分割;姚等提出了一個新的全自動勾畫心內膜算法[4],該算法應用中心起源的心形搜索,用改進的Sobel算子進行放射形邊界探測,并且依據相鄰離心距差進行邊界點修正。通過對12幅質量不同的超聲圖像進行實驗,準確率達到了56%,已經是比較好的效果。
心臟的運動是永不停息的,所以僅對某一時刻的靜態圖像分析是遠遠不夠的,本文采用高解析度的M型超聲成像,應用類似腹部超聲顯像中所使用的標準的B掃描聲像儀,用心電圖作為顯波顯像的控制閘門,記錄心動周期中每一個舒張或收縮狀態,集合許多心動周期成一個斷面圖像[5]。本文以此作為原始材料進行研究,在進行自適應閾值的簡單預處理后,應用改進的CV水平集方法進行實驗,力求從另外的方向來精確地提取左心室的內、外膜邊緣,進而進行參數測量等后續工作。
1 改進的CV水平集算法
活動輪廓模型是基于邊緣像素信息的,傳統的CV模型是基于區域信息的,但是前提是區域是同質的,即假設同一區域內像素強度均一[6],但實際應用中,由于技術限制或采集時的人為原因,多數醫學圖像都很難達到區域同質的要求,比如本文討論的心室心肌纖維層。Li Chunming[7]等提出了一種基于區域擴展性擬合能量的水平集算法,提出了一個RSF擬合區域擴展性能量函數,以一個邊界輪廓C和在近似邊界兩端圖像強度的兩個擬合函數f1(x)和f2(x)來定義,區域擴展的能量依賴于特定參數的核函數,利用可控范圍內區域強度信息,從小的領域擴展到整個的圖像域,然后將這個能量并入到變水平集公式中,最終曲線經演化獲得能量函數的極小化值,應用可控范圍的局部區域強度信息來計算這兩個擬合函數,引導曲線擴展向目標的邊界。

實驗過程中首先采用隱性活動輪廓將初始輪廓標記圖上,基于此進行水平集演化。此外,參數的設定對圖像分割結果影響較大。本文在參數λ1和λ2的選擇上進行了部分研究,由于能量函數值是由輪廓內部和外部兩部分決定,如果取λ1=λ2,則拓撲同時發生,朝向整個圖像。而為了剔除非心肌組織的干擾,需要拓撲向輪廓限制區域內,即設定了2λ1=λ2。
2 實驗及仿真結果
圖1所示為一張包含4個心動周期的心室肌舒張和收縮過程的經食道胃底短軸切面超聲圖像。從圖中可看到,中空部分的上下兩側是由很多層心肌纖維層組成的左心室心肌,這樣的層結構導致左心室心肌剖面圖像的灰度是明暗相間的,也就是說心肌區域是灰度不均勻的,這在圖像分割上是一個很大的難題。
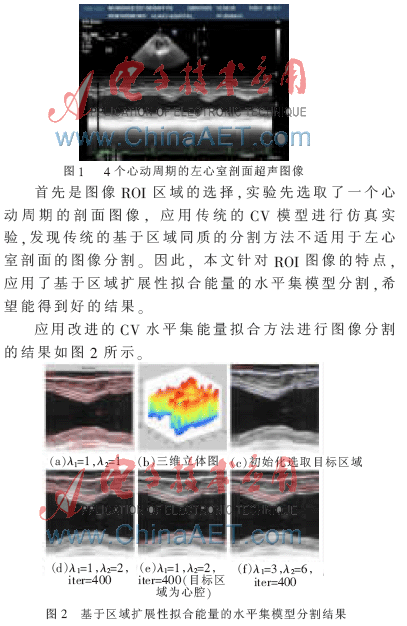
以上仿真中σ取3.0,比較結果可得,本文應用基于隱性區域擴展性擬合能量的水平集模型分割取得了預期的結果,分割效果比較滿意。實驗中參數的設定包括迭代次數、λ1和λ2,比較圖2(a)和(f),若λ1=λ2=1,則拓撲向整個圖像,這樣的多目標尋找與多相位方法優缺參半,對于圖2(e)和(f),若設定2λ1=λ2=2和2λ1=λ2=6的兩種情況,心肌邊緣清晰可見,完全濾掉了腱索和肌小梁的干擾。實驗對原圖像4個周期的ROI進行分析,設定λ1=3,λ2=6,iter=400,圖3為另外3個心動周期的仿真結果,除了第4個周期的圖像效果較差外,其他的圖像都能準確得到心室上邊界的內外膜。M型超聲隨時間變化而高速采樣,時間越長,圖像的效果越差,造成分割的困難,而對于左心室下半部分,從4個周期可見,邊界都比較模糊,暫不做分析。基于隱性的區域擴展性擬合能量的水平集模型分割實現了準確提取上半部分的內外膜目的。這樣的分割的方法同時應用于心室邊界。分割還需要結合醫生的經驗,來識別正確的邊緣,以免出現誤分割。
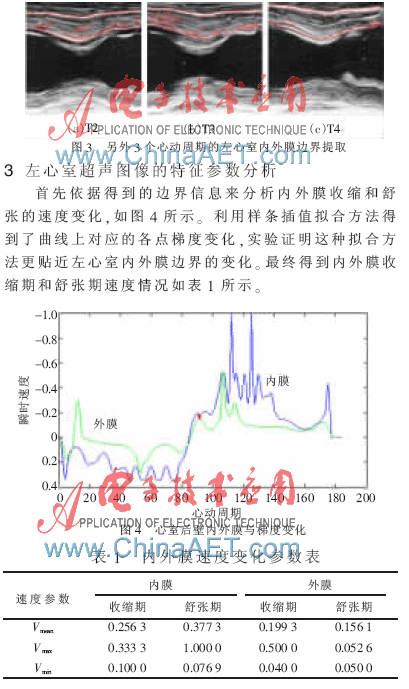
由表1可見,心室外膜的速度變化小于內膜的速度變化,對于心室內膜還可以得出心肌收縮階段的平均速度變化要小于舒張階段,舒張過程在加速,但在收縮末期附近速度變化比較均勻,而在舒張的末期會出現速度變化比較大的情況。由4個周期分割后的邊界輪廓還可以得到,內膜收縮時間和舒張時間比約為9:10,這與正常心動周期內舒張過程比收縮過程長是一致的,這樣既有利于血液流回心臟,又能使心肌有充分的時間休息。
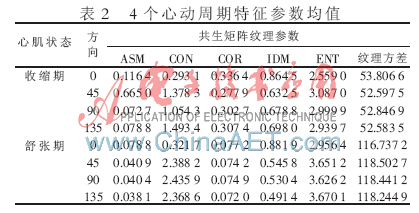
接著進行了舒張期與收縮期紋理比較。首先采用共生矩陣方法,如表2所示,從4個方向進行紋理灰度共生矩陣統計后各個值。為了統計各參數的影響,選取了4個周期的狀態最后各參數取平均值。
由表2可以分析得出,除了IDM相差不大外,其他參數(如對比度、角二階矩和相關等)均相差較大,其中在水平方向上,收縮期與舒張期的對比度相差不大,但在其他方向上有COND>CONS,這表明在取樣區域內舒張期出現了大的灰度差異頻移,而收縮期內的紋理相對細膩柔和,與人眼的感知相符。同時,對于角二階矩ASMS>ASMD,也反映收縮過程中的紋理是規則變化的。兩個過程圖像的熵和紋理方差都有一定差異,這都反映出了心肌緊縮階段的紋理變化比較均勻。分析引起該狀況的原因主要是:收縮期心肌增厚,小梁相互交叉,心肌分層達最大值,層與層之間的力學特征基本一致,比較舒張過程中心肌之間的回聲一致性下降的結果。
另一方面,由于分形維數直觀上與物體表面的租糙程度相吻合,而自然界中的不同物體租糙度有很大差別,可用分形維數作為區分不同類別物體的有效參數。因此如何準確地估計計算分形維數成為研究的重點。本文應用差分盒維數法,采集到的2個心動周期的左心室舒張收縮過程AVI幀進行分析,找到整個過程的分形值的規律,然后再比較舒張過程和收縮過程心室壁的分形維信息,找到它們之間的聯系。
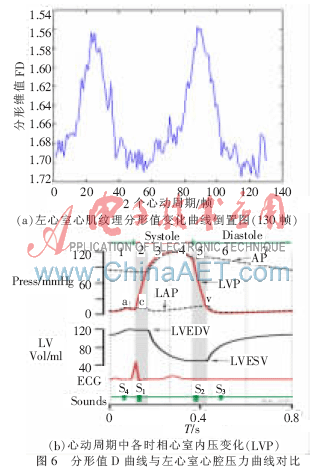
在提取了二維B超心室心肌收縮和舒張過程中AVI幀后,選取了一個完整的心動周期的左心室圖像,圖5(a)、(b)顯示的是舒張末和收縮末左心室的形態及紋理。選取了一個心動周期共55幀B超圖像來計算左心室的分形維數,得到的差分分形維數FD值曲線(圖5(c)),可以看到分形維的變化:在心肌收縮末點時最小,舒張末取得最大值,有FDmax=1.715 7、FDmax=1.556 7。
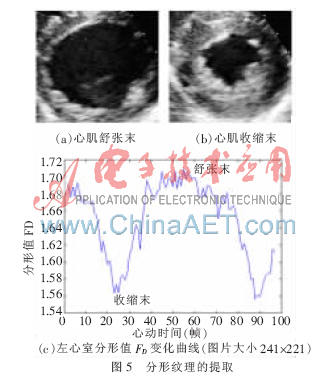
從曲線走勢來看,在收縮過程中的值是下降的,舒張過程中是上升的,也可以得出舒張過程的時間要長于收縮時間。這與之前分割出來的心室內膜邊界的走勢是極為相似的,與參考文獻[8]中是利用聲學造影劑后得出的結論基本一致。
另外,比較如圖6(b)(圖片來源于維基百科left ventricular pressure)心動周期各時相心室內壓所示,心室在心動周期中的壓力變化在收縮期和舒張期也體現的比較明顯,具體為:心室肌的收縮使室內壓突然增加,等容收縮期內心室內壓上升的速率加快,當心室收縮結束,立即開始心室舒張,室內壓會下降,在等容舒張期內左心室內壓急劇下降。這一過程與圖5中分析的分形值的反向變化(圖6(a)所示)趨勢相關,推測可以進一步應用分形維在估計心室壓力曲線的變化值。
為了比較左心室超聲心動圖心肌纖維層的紋理變化,本文進行了統計,計算心室收縮過程的25幀圖像與舒張過程中的30幀圖像各自的平均分形維數,結果如下:mean(FDS)=1.644 1<mean(FDD)=1.661 8,而統計之前圖6中的紋理分形維,也可以得出收縮過程的分形維均值小于舒張過程的分形維均值,分形維在一定程度上也反映了圖像的信息量,與本文利用共生矩陣得出的統計特性基本一致。
M型超聲心動圖最早應用于心臟結構的探測,隨著現代科學技術的發展,尤其是解剖型、全方向M型超聲的發展,使得M型超聲圖像的每秒掃描取樣線大大增加,因而更能準確掌握室壁在心動周期不同時相中的活動規律,了解心壁各層在收縮期跨壁速度梯度的差異。由于圖像紋理灰度的差異不同,因而醫學分割方法不盡相同。本文針對結構復雜的左心室剖面,在分析前首先找出心肌組織,應用改進的CV水平集方法,基于區域擴展性擬合能量的水平集模型,通過更改參數準確得到了心室的內外膜的邊界,從而為后面的特征分析奠定了基礎。最后,重點對心肌收縮和舒張過程的紋理變化作比較分析,得出了心肌運動的過程中收縮期和舒張期的時間、共生矩陣各特性參數、分形維等均有差別,可為醫生的臨床診斷提供參考。
參考文獻
[1] FOLLAND E D, PARISI A F, MOYNIHAM P F, et al. Assessment of left ventricular ejection fraction and volumes by real time two dimensional ec-hocardiography: a comparison of cineangio-graphic and radionuclide techniques[J]. Circ, 1979, 60 (4): 760-766.
[2] KRIPS R, ADAM D R. Left ventricular wall segmentation in ultrasound cross-sectional images computer in cardiology in 1996[C]. IEEE Conference, 1999: 141-144.
[3] LACERDA S G, DA ROCHA A F, VASCONCELOS D F, et al. Left ventricle segmentation in echocardiography using a radial-search based image processing algorithm[C]. 30th An-nual International Conference of IEEE EMBS 2008, 2008:222-225.
[4] 姚煒,田建明,趙寶珍,等.關于一個全自動勾畫超聲左心室內膜算法的初步研究[J].中國超聲醫學雜志,2002,18(10).
[5] 徐智章.左心室超聲心動圖檢查[J].國際心血管病雜志:1975(5).
[6] VESE L A, CHAN T F. A multiphase level set framework for image segmentation using the Mumford and Shah model[J]. International Journal of Computer Vision, 2002,50(3):271-293.
[7] Li Chunming, Kao Chiuyen, GORE J C, et al. Minimization of Region- Scalable Fitting Energy for Image Segmentation[J]. IEEE Transactions on Image Processing 2008, 17:1940-1949.
[8] SARKAR N, CHAUDHUTIB B. An efficient approach to estimate fractal dimension of textural images[J]. Pattern Recognition, 1992, 25(9):1035-1041.

